Objetivos
Se estima que la enfermedad pulmonar obstructiva crónica (EPOC) afecten a más de 500 millones de personas en todo el mundo, causando discapacidad, pérdida de calidad de vida y carga social significativas, con costes que superan los € 56 mil millones al año en la Unión Europea (UE) [Decramer et al.]. Proyecciones recientes apuntan que será la tercera causa de mortalidad mundial para el año 2030. Se caracteriza por una respuesta inflamatoria que induce la remodelación de la vía aérea, limitación del flujo aéreo y una función pulmonar disminuida. Las terapias actuales tienen un impacto inadecuado sobre la evolución y la mortalidad en la EPOC [Martinez et al.] debido a la incompleta comprensión de la fisiopatología y la falta de reconocimiento de la heterogeneidad, complejidad y multi-escala de estas enfermedades, ya que son causadas por una variedad de interacciones entre los genes y el ambiente. No existe una sola diana terapéutica que dé resultado en todos los pacientes y por eso el objetivo general del proyecto INSPIRE es caracterizar esta heterogeneidad específica del paciente utilizando modelos computacionales, datos moleculares y de imágenes médicas, con el fin de adecuar las opciones terapéuticas con el fenotipo del paciente y su perfil de riesgo.
Hipótesis 1 - Se pueden establecer y validar vínculos racionales entre fenotipos de pacientes y mecanismos celulares claves en el desarrollo de EPOC: Las patogénesis de la EPOC son poco conocidas. Sin embargo, se cree que sean dirigidas por una serie de procesos celulares multi-escala, incluyendo la inflamación de las vías respiratorias, la adaptación y la inmunidad innata al consumo de cigarrillos, sensibilidad a antígenos propios o externos, senescencia acelerada y desregulación de los mecanismos de reparación 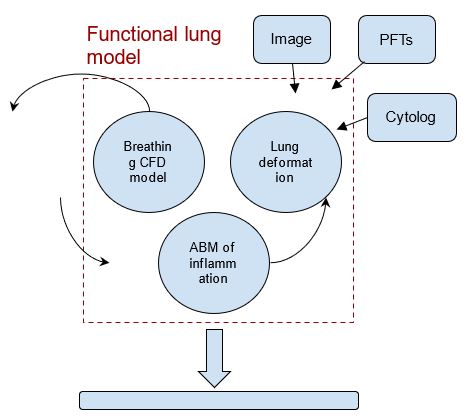 celular [Repapi et al., Pavord et al.]. Finalmente, una variedad de genes candidatos recientemente han sido reportados en estudios de asociación del genoma [Akinbami et al.]. El uso constante de corticosteroides inhalados y un reconocimiento más amplio de marcadores asociados con el riesgo adverso [Partridge et al.], reduce la mortalidad de estas enfermedades, pero muchos pacientes siguen teniendo exacerbaciones y un mal control de los síntomas [Brightling et al.]. Sin embargo, se ha demostrado que terapias dirigidas a diferentes fenotipos de manera específica reducen las exacerbaciones [Holgate et al., Castro et al.].
celular [Repapi et al., Pavord et al.]. Finalmente, una variedad de genes candidatos recientemente han sido reportados en estudios de asociación del genoma [Akinbami et al.]. El uso constante de corticosteroides inhalados y un reconocimiento más amplio de marcadores asociados con el riesgo adverso [Partridge et al.], reduce la mortalidad de estas enfermedades, pero muchos pacientes siguen teniendo exacerbaciones y un mal control de los síntomas [Brightling et al.]. Sin embargo, se ha demostrado que terapias dirigidas a diferentes fenotipos de manera específica reducen las exacerbaciones [Holgate et al., Castro et al.].
Hipótesis 2 - Es posible usar un modelo computacional multi-escala y multi-resolución para capturar los mecanismos esenciales de COPD. Recientes avances interdisciplinares en fisiología, radiología, análisis de imágenes, bioingeniería, modelización computacional y biología de sistemas han permitido empezar el desarrollo de un modelo integrado de escala múltiple de las vías respiratorias con el fin de desentrañar los complejos mecanismos fisiopatológicos que ocurren en la EPOC. Por ejemplo [Bordas et al.] describe cómo obtener una malla específica del paciente para simulaciones de CFD utilizando Ansys y en [Berger et al. se discute la aplicación de un modelo de deformaciones poroelástico para la ventilación pulmonar. [Chernyavsky et al.] describe un modelo teórico del posible efecto de la inflamación sobre el restringimento de las vías pequeñas. Una revisión completa del estado del arte actual y de las posibles vías de trabajo futuro es en [Burrowes et al 2013].
Avances con respecto al estado del arte: A través de la verificación de estas dos hipótesis, el proyecto INSPIRE se propone avanzar el estado del arte en el conocimiento y en la técnica en numerosos puntos. Primero, aprovechando la experiencia del BSC en supercomputación y generación de mallas nos proponemos obtener un proceso de mallado con resolución y calidad mejor de las que están disponibles. Además gracias al trabajo conjunto con la UPF, no será necesario recrear la malla en su totalidad por cada nuevo paciente, sino que se usarán metodologías de registro para adaptarlas a los nuevos pacientes, mediante un proceso de deformación continua de malla de volumen desarrollado en el BSC. También, en lugar de usar un solver comercial, el BSC desarrollará los modelos para su solver interno Alya, cosa que permitirá mayor flexibilidad a la hora de definir las propiedades avanzadas de los tejidos así como una mayor fidelidad de los resultados puesto que la precisión con la que se resuelve el complejo flujo en las vías respiratorias supera el estado del arte actual. Como punto adicional, procederemos a implementar los modelos teóricos existentes el literatura entre inflamación y restricción de las vías aéreas con códigos basados en agentes, con especial atención al papel que juega el sistema inmunitario. Finalmente, las escalas más macroscópicas, i.e. tejido y órgano no suelen estar acopladas en los modelos descritos anteriormente. Por lo tanto éstos tampoco tienen en cuenta el importante feedback iterativo que existe entre las escalas celulares y moleculares y las escalas macroscópicas, mientras este feedback es clave para la personalización de modelos y de las predicciones en base a fenotipos de pacientes clínicamente observables. Tal integración, para la cual un alto poder computacional es imprescindible es la que proponemos implementar y validar en términos de fenotipos de pacientes a lo largo del tiempo. Tal validación aportará una prueba de concepto fundamental para el uso de model en la mejora de la clasificación de los pacientes y estratificaciones de su perfil de riesgo, teniendo en cuenta la complejidad biológica de la EPOC.
El subproyecto 2 tiene como finalidades:
- (i) El modelado multiescala de los mecanismos de progresión avanzada de la enfermedad pulmonar obstructiva crónica basado en evidencias clínicas, mecánicas y biológicas. Este acople dependerá de la capacidad del modelo de agentes de celular alveolar para generar inflamación y responder a dicha inflamación en un entorno mecánico concreto. Este entorno será parcialmente controlado por la regulación de la composición del tejido alveolar, de acuerdo con las predicciones del mismo modelo de agente.
- (ii) Crear un modelo HPC FEM del estrés en los pulmones causado por la respiración. Este modelo tendrá en cuenta las presiones locales generadas por los flujos de aire y la simulación del tejido alveolar dominado por el balance entre fibras de colágeno y de elástina [Wier]. Este objetivo requerirá una gran interacción con el BSC.
- (iii) Crear un modelo predictivo del fenotipo de los pacientes de EPOC utilizando escan de CBCT. Estos datos consisten en un conjunto de 220 pacientes entre 40-80 años con EPOC representativos de todos los estadios GOLD participantes en un programa internacional de cribado de cancer de pulmon (I-ELCAP). Cada paciente tiene un scan CT de baja resolución basal más una repetición anual. La Clínica Universidad de Navarra (CUN) permitirá el acceso a estos datos para validar los resultados de INSPIRE (ver carta EPO al final de la propuesta), lo cual será facilitado mediante la participación en el equipo de trabajo del Subproyecto 1 de Jessica González Gutiérrez, licenciada en Medicina y Cirugía, y miembro de la CUN.
La validación directa de los modelos o sistemas de modelos teóricos que pretenden simular sistemas complejos no siempre es factible, ya que sistemas estocásticos y determinísticos, con y sin incertidumbre respectivamente, pueden dar diferentes resultados al ser usados para simular el mismo fenómeno biológico (Paradoja de Keizer) [Walpole et al]. No obstante, estudios de la sensibilidad a variaciones de parámetros y posibles calibraciones de parámetros de modelo frente a mediciones, permiten validar la relevancia física y la certitud teórica de las hipótesis de modelización. En este sentido, los mecanismos descritos por el comportamiento de los modelos a lo largo de las simulaciones son dignos de consideración para investigar relaciones no anticipadas entre fragmentos de evidencias, y diseñar experimentos para comprobar nuevas hipótesis.
La capacidad de los modelos para describir fenómenos complejos crece indudablemente con la adecuación de las adquisiciones de evidencias a las hipótesis de modelización. Por lo tanto este subproyecto pretende estudiar los mecanismos de evolución de la EPOC en paralelo con un conjunto de imágenes provenientes por un estudio clínico retrospectivo.
Para alcanzar las metas propuestas, los objetivos específicos del subproyecto 2 son:
- Establecer un esquema de regulación biológica de los mecanismos inmunológicos y celulares de la inflamación continua en el epitelio pulmonar implementado en un modelo basado en agentes (BA) para predecir la pérdida de las vías aéreas pequeñas (bronquiolitis) y la remodelación y destrucción del parénquima pulmonar (enfisema). Este esquema será implementado en un modelo de agentes celulares alveolares.
- Construcción de modelos elementos finitos (EF) de la respiración en el pulmón de sujetos sanos, incluyendo la geometría de las vías aéreas. Teniendo en cuenta las deformación típica de los proceso de ventilación pulmonar y la elasticidad residual de las paredes alveolares afectadas por enfisema.
- Aplicar técnicas de aprendizaje automático para crear un modelo predictivo que pueda clasificar el fenotipo de los paciente aprendiendo de un conjunto de datos retrospectivos de 220 pacientes.
- Cuantificar cuál sería el valor añadido de personalizar el tratamiento de la EPOC utilizando los datos clínicos retrospectivos de pacientes.
