Movimiento celular bajo presión
Un equipo internacional de científicos ha definido el mecanismo molecular que impulsa el movimiento celular en entornos extremadamente estrechos por los cuales habitualmente tienen que desplazarse en las células.

Un equipo internacional de investigadores en el que participan la Dra. Selma A. Serra y el Dr. Miguel A. Valverde del Departamento de Ciencias Experimentales y de la Salud (DCEXS) de la UPF muestra por primera vez el mecanismo empleado por las células para decidir qué dirección tomar cuando se desplazan por los intrincados recovecos del organismo.
Uno de los procesos más básicos en nuestros cuerpos es cómo las células se mueven por los diferentes tejidos. Este comportamiento es esencial para nuestra supervivencia, por ejemplo, para curar heridas, pero también puede conducir a la diseminación de las células tumorales y la aparición de metástasis.
Nuestro conocimiento sobre los principios que guían la migración celular crece constantemente. Sin embargo, aún no tenemos respuesta a algunas preguntas fundamentales, tales como qué tipo de información utilizan las células para determinar la dirección de su movimiento.
Han demostrado que a l'hora de decidir una dirección las células prefieren desplazarse hacia caminos en los que haya menor resistencia hidráulica, aunque sean caminos más angostos.
La investigación realizada en la Universidad Johns Hopkins (Baltimore, EE. UU. y UPF ha definido el mecanismo molecular que impulsa el movimiento celular en entornos extremadamente estrechos por los que habitualmente tienen que desplazarse las células. El estudio publicado en Science Advances ha demostrado que a la hora de decidir una dirección las células prefieren desplazarse hacia caminos en los que haya menor resistencia hidráulica, aunque sean caminos más angostos.
¿Qué determina la dirección que toma una celda en una intersección? Al igual que nosotros, parados frente a caminos que se cruzan, las celdas evalúan diferentes parámetros, como la dificultad o el atractivo de la ruta para elegir el camino.
Se sabe mucho sobre la química (presencia de quimioatrayentes) y las señales físicas (interacciones con la matriz extracelular) que guían el movimiento de las células normales y las células cancerosas. En sus estudios, investigadores de las Universidades Johns Hopkins y UPF analizaron el movimiento de las células en andamiajes generados utilizando técnicas de bioingeniería para diseñar túneles que presentaban diferentes anchuras y resistencias/presiones hidráulicas (que es la resistencia que experimenta una célula al desplazar la columna de agua dentro de un tubo.
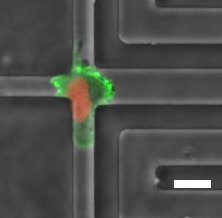 Estos dispositivos, además de permitir confinar de forma controlada las células de igual forma que acontece en nuestro organismo, permiten que los investigadores puedan analizar las respuestas eléctricas y el flujo de iones que se producen en las células. En sus estudios, los investigadores también incluyeron un parámetro físico que es notablemente más alto en los tumores que en tejidos sanos, la presión del fluido —también expresada como resistencia hidráulica—, y del que no se sabía mucho a cerca de su impacto en el movimiento celular. La presión del fluido es solo una de las muchas fuerzas en un tumor que puede influir en su desarrollo y progresión. Por lo tanto, comprender cómo las células detectan y responden a la presión del fluido es importante en el contexto de la biología del cáncer.
Estos dispositivos, además de permitir confinar de forma controlada las células de igual forma que acontece en nuestro organismo, permiten que los investigadores puedan analizar las respuestas eléctricas y el flujo de iones que se producen en las células. En sus estudios, los investigadores también incluyeron un parámetro físico que es notablemente más alto en los tumores que en tejidos sanos, la presión del fluido —también expresada como resistencia hidráulica—, y del que no se sabía mucho a cerca de su impacto en el movimiento celular. La presión del fluido es solo una de las muchas fuerzas en un tumor que puede influir en su desarrollo y progresión. Por lo tanto, comprender cómo las células detectan y responden a la presión del fluido es importante en el contexto de la biología del cáncer.
Los investigadores descubrieron que las células de cáncer de mama toman decisiones a la hora de escoger la dirección de su movimiento basadas en las diferentes resistencias hidráulicas que detectan en los puntos de intersección de los túneles a través de los que se desplazan. También querían saber qué mecanismo molecular era responsable de la detección de la resistencia hidráulica y su acoplamiento con la maquinaria del citoesqueleto, que en última instancia dictará la dirección de movimiento de la célula.
Para ello, analizaron la contribución de diferentes canales iónicos que son proteínas que se encuentran en la membrana plasmática y están especializados en responder rápidamente a los cambios en las condiciones físicas del medio ambiente. La activación de estos canales de iones genera corrientes eléctricas (producida por el movimiento de los iones) y la entrada de calcio dentro de la célula. Este ión de calcio a su vez activa la formación de un escudo hecho de los componentes esqueléticos de la célula (las proteínas actina y miosina) que protege contra las fuerzas externas (hidráulicas) y redirige la entrada de la célula en canales de baja resistencia, a pesar de que son más estrechos que aquellos de mayor resistencia hidráulica. Los investigadores identificaron el canal iónico TRPM7 como el sensor molecular que detecta cambios en la presión hidráulica / hidrostática y promueve la entrada de calcio que, en última instancia, determina la toma de decisiones de las células en las intersecciones.
Analizaron el movimiento de las células en andamiajes generadas utilizando técnicas de bioingeniería para diseñar túneles que presentaban diferentes anchuras y resistencias o presiones hidráulicas.
Esta investigación es la continuación de una fructífera colaboración que se inició hace cuatro años entre el laboratorio de bioingenieros de la Universidad Johns Hopkins y el laboratorio de fisiólogos moleculares de la UPF. “Nuestro objetivo de futuro es comprender cuales son todos los mecanismos moleculares que intervienen en el control del movimiento celular en entornos confinados para comprender cómo las células tumorales invaden y metastatizan” afirma Valverde.
Financiado por:
National Institutes of Health (USA), Ministerio de Ciencia, Innovación y Universidades (España), el Programa “Maria de Maeztu”para unidades de Excelencia al Departamento de Ciencias Experimentales y de la Salud de la UPF, y fondos FEDER.
Artículo de referencia:
Cell Sensing and Decision-Making in Confinement: The role of TRPM7 in a tug of war between hydraulic pressure and cross-sectional area. By Runchen Zhao, Alexandros Afthinos, Tian Zhu, Panagiotis Mistriotis, Yizeng Li, Selma A. Serra, Yuqi Zhang, Christopher L. Yankaskas, Shuyu He, Miguel A. Valverde, Sean X. Sun, and Konstantinos Konstantopoulos. Science Advances, July 2019 DOI: 10.1126/sciadv.aaw7243.
