La interacción entre canales, receptores y la progesterona facilitan el transporte de huevos y embriones en las trompas de Falopio
La interacción entre canales, receptores y la progesterona facilitan el transporte de huevos y embriones en las trompas de Falopio
El estudio, dirigido por Miguel Angel Valverde del Laboratorio de Fisiología Molecular de la UPF, ha sido publicado en Science Signaling.
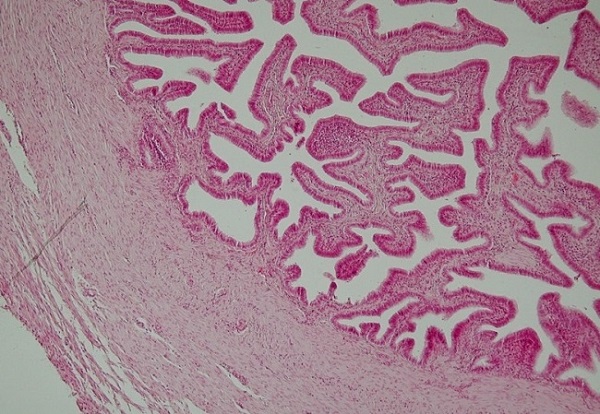
Las trompas de Falopio (también conocidos como oviductos) son dos tubos estrechos y largos que conectan los ovarios con el útero. Desempeñan un papel esencial en el transporte de huevos, la fertilización y el desarrollo temprano del embrión. A menudo, el proceso de fertilización ocurre dentro de estos tubos, seguido del transporte del óvulo fecundado al útero. Cuando este proceso se altera y un óvulo fecundado se implanta fuera del útero, generalmente en el oviducto, se produce un embarazo ectópico que puede poner en riesgo la vida de la madre. Por lo tanto, es de gran interés conocer los factores que controlan el transporte de huevos a través de este tubo estrecho.
Un factor que afecta la función de la trompa de Falopio es la progesterona. La progesterona es una hormona reproductiva. Su receptor, una proteína expresada en tejidos como el útero, el ovario y el cuello uterino, se une a la hormona y envía señales que preparan a las mujeres y sus tejidos reproductivos para el embarazo. La progesterona también está presente a altas concentraciones en las secreciones ováricas en el oviducto y el peritoneo. En el oviducto afecta a las células musculares y epiteliales, así como a los espermatozoides. Los primeros estudios realizados en la década de los 70 mostraron que los progestágenos aceleraron el transporte de óvulos desde el oviducto hasta el útero, mientras que los estudios más recientes informaron que en respuesta a la progesterona se produce una disminución de la frecuencia del batido ciliar (FBC) en las células ciliadas del oviducto. Esta aparente controversia llamó nuestra atención para comenzar a investigar el papel de la progesterona en el oviducto", dice Valverde.
Esta investigación ha identificado una interacción funcional sin precedentes de tres proteínas de membrana para acelerar el latido de los cilios en respuesta a la progesterona.
El estudio se publica este mes en la revista Science Signaling y en él participan investigadores del Laboratorio de Fisiología Molecular del Departamento de Ciencias Experimentales y de la Salud de la Universidad Pompeu Fabra y la Unidad de Farmacología del IDIBELL-Universitat de Barcelona.
Muchas células que recubren las vías respiratorias y el tracto reproductivo contienen proyecciones llamadas cilios, cuya función es, en el caso de las vías respiratorias, eliminar partículas extrañas, agentes patógenos y alérgenos. El fracaso de esta acción ciliar contribuye a la patología respiratoria. Del mismo modo, el transporte de gametos y embriones a través del tubo de Falopio también depende de la actividad ciliar. El efecto de propulsión ejercido por los cilios depende de diferentes factores, uno de los más importantes es un aumento en la concentración de calcio intracelular y la posterior aceleración de la frecuencia de batido ciliar. El Laboratorio de Fisiología Molecular de la UPF ya había identificado previamente una de las proteínas clave que forman la vía para la entrada de calcio, controlando así la actividad ciliar.
El estudio abre nuevas líneas de investigación sobre posibilidades terapéuticas para abordar las disfunciones en el transporte de óvulos en el oviducto.
Los investigadores primero mostraron que coexisten dos patrones diferentes de acción de la progesterona en el control de la FBC en células oviductales ciliadas: un efecto a corto plazo (no genómico) caracterizado por la generación de señales de Ca2+ y un rápido aumento de la FBC, y un efecto a largo plazo caracterizado por una disminución de la FC y la participación del receptor de progesterona clásico.
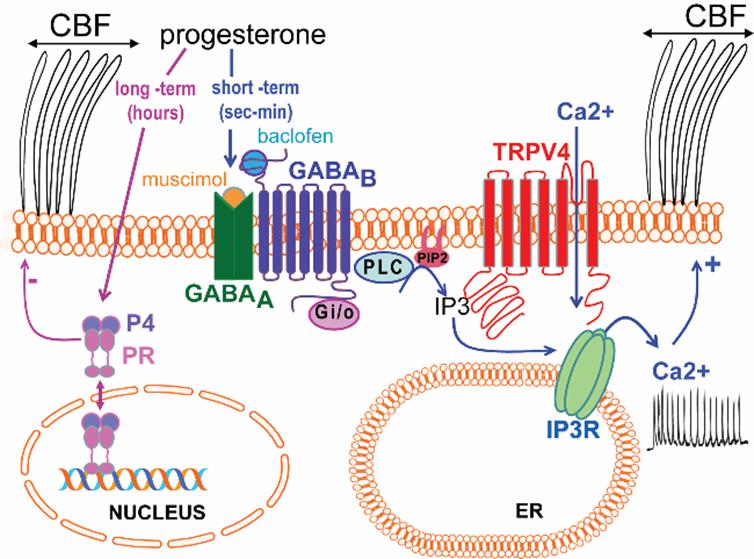 En segundo lugar, han delineado un mecanismo molecular novedoso por el cual la progesterona rápidamente (efecto a corto plazo) aumenta el Ca2+ intracelular y acelera CBF, un mecanismo que implica la activación gradual de los receptores para un neurotransmisor que principalmente se encuentra en el cerebro, GABAA y GABAB, y para los cuales no se tienen una idea clara de su función fuera del sistema nervioso. El estudio ahora publicado demuestra que la unión de la progesterona al GABAA transactiva los receptores GABAB acoplados a proteína Gi/o y genera señales de Ca2+ mediadas por IP3. Además, los investigadores mostraron que para ser funcional, este mecanismo requiere la actividad basal del canal TRPV4 para proporcionar flujo de entrada de Ca2+ en las proximidades del receptor de IP3, promoviendo así la iniciación y el mantenimiento de las señales oscilantes de Ca2+ necesarias para acelerar la FBC.
En segundo lugar, han delineado un mecanismo molecular novedoso por el cual la progesterona rápidamente (efecto a corto plazo) aumenta el Ca2+ intracelular y acelera CBF, un mecanismo que implica la activación gradual de los receptores para un neurotransmisor que principalmente se encuentra en el cerebro, GABAA y GABAB, y para los cuales no se tienen una idea clara de su función fuera del sistema nervioso. El estudio ahora publicado demuestra que la unión de la progesterona al GABAA transactiva los receptores GABAB acoplados a proteína Gi/o y genera señales de Ca2+ mediadas por IP3. Además, los investigadores mostraron que para ser funcional, este mecanismo requiere la actividad basal del canal TRPV4 para proporcionar flujo de entrada de Ca2+ en las proximidades del receptor de IP3, promoviendo así la iniciación y el mantenimiento de las señales oscilantes de Ca2+ necesarias para acelerar la FBC.
Esta investigación ha identificado una interacción funcional sin precedentes de tres proteínas de membrana para acelerar el latido de los cilios en respuesta a la progesterona: dos tipos de receptores para un neurotransmisor típicamente asociado a la función cerebral (GABA) y un canal de iones (TRPV4) con un papel destacado en la regulación de epitelio ciliado. Además, “el estudio abre nuevas líneas de investigación sobre posibilidades terapéuticas para abordar las disfunciones en el transporte de óvulos en el oviducto ", dice Valverde.
Artículo de referencia:
C. Jung, V. Fernández-Dueñas, C. Plata, A. Garcia-Elias, F. Ciruela, J. M. Fernández-Fernández, M. A. Valverde. Functional coupling of GABAA/B receptors and the channel TRPV4 mediates rapid progesterone signaling in the oviduct. Sci. Signal. 11, eaam6558 (2018). DOI: 10.1126/scisignal.aam6558
